Fernando Galán Galán
Profesor Titular de Medicina
Especialista en Medicina Interna
Experto en Miopatía Mitocondrial del Adulto
Fibromialgía y Síndrome de Fatiga crónica
BLOG
FOSFORILACIÓN OXIDATIVA: CADENA DE TRANSPORTE DE ELECTRONES O CADENA RESPIRATORIA MITOCONDRIAL
TRAS LA INTRODUCCIÓN Y ACLARACIONES DE CONCEPTOS EN EL ARTÍCULO ANTERIOR, ESTAMOS YA EN DISPOSICIÓN DE EXPLICAR Y ESPERO QUE USTEDES, ENTENDER.
La fosforilación oxidativa es simple en cuanto a concepto, pero compleja en cuanto al mecanismo.
CADENA DE TRANSPORTE DE ELECTRONES O CADENA RESPIRATORIA MITOCONDRIAL
Es una cadena de reacciones redox (de oxidación y reducción) en la que hay interacción sucesiva de portadores que transfieren electrones, que se asemejan a una carrera de relevos en la que los electrones pasan rápidamente de un componente a otro, hasta el punto final de la cadena, donde los electrones reducen el oxígeno molecular y producen agua
Componentes
Todos los componentes se encuentran en la membrana mitocondrial interna (MMI)
que contiene 5 complejos:
- Complejo multienzimáticos I, II, III, IV
- Complejo V (ATP sintasa: cataliza la síntesis de ATP)
Portadores de electrones móviles
- CoQ
- Citocromo c
Organización
- Cada complejo acepta o dona electrones a portadores móviles.
- Los portadores aceptan electrones de los donantes y luego donan al siguiente portador en cadena.
- Los electrones finalmente se combinan con oxígeno y protones para formar agua.
- Se requiere oxígeno como aceptor final (cadena respiratoria).
Los Complejo multienzimáticos están compuestos por subunidades proteicas codificadas por el ADN mitocondrial y ADN nuclear. Los complejos I, III y IV se encuentran atravesando la membrana interna mitocondrial, mientras que el complejo II está tan solo anclado a ella.
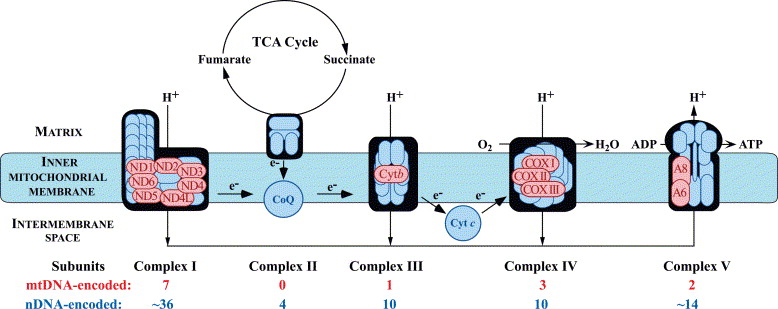
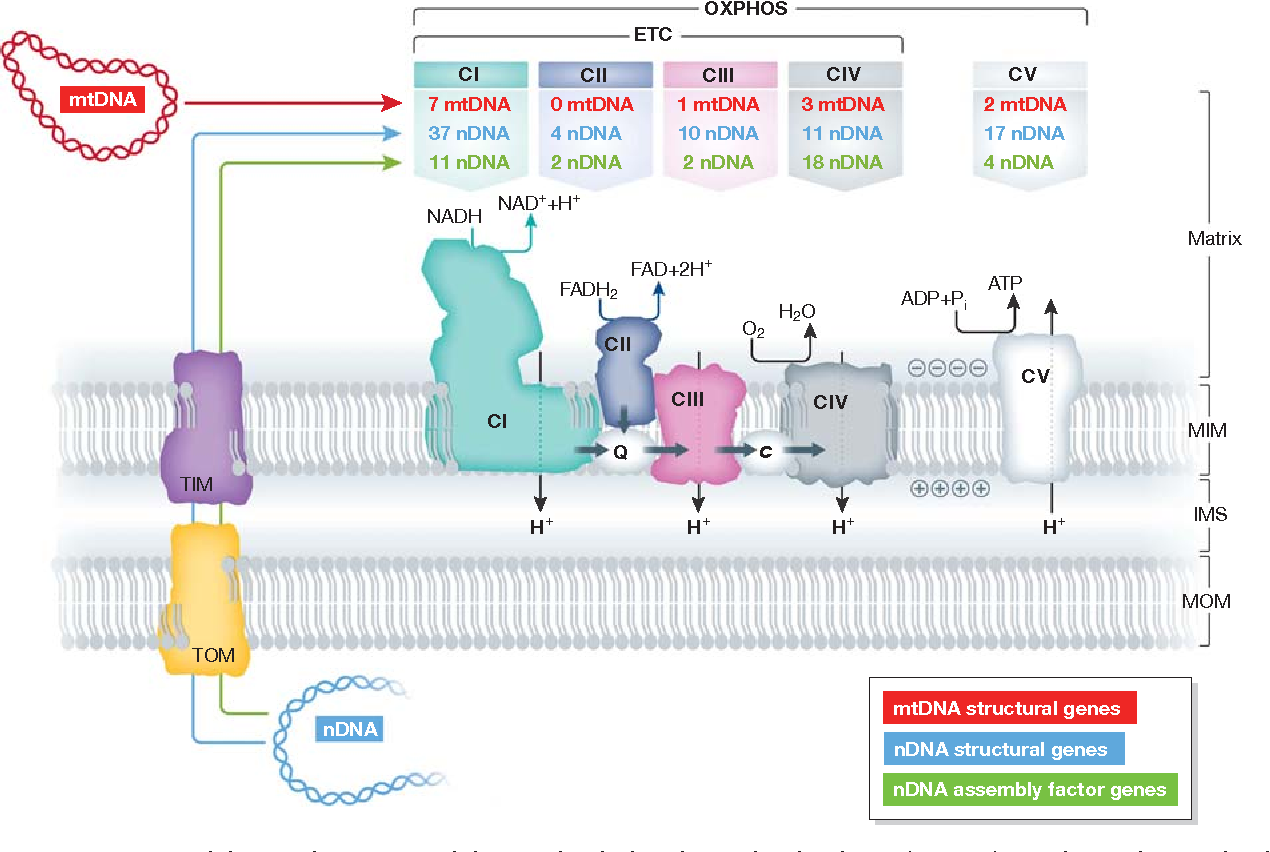
Las subunidades de CI, CIII, CIV y CV están codificadas por el ADN mitocondrial (ADNmt; rojo) y el ADN nuclear (nDNA; azul), mientras que la CII consiste exclusivamente en subunidades codificadas por el nDNA. La biogénesis está mediada por factores de ensamblaje codificados por DNA nuclear (verde). Las proteínas codificadas por nDNA se importan a la matriz mitocondrial a través de los sistemas TOM (translocador de la membrana interna) y TIM (translocador de la membrana interna).
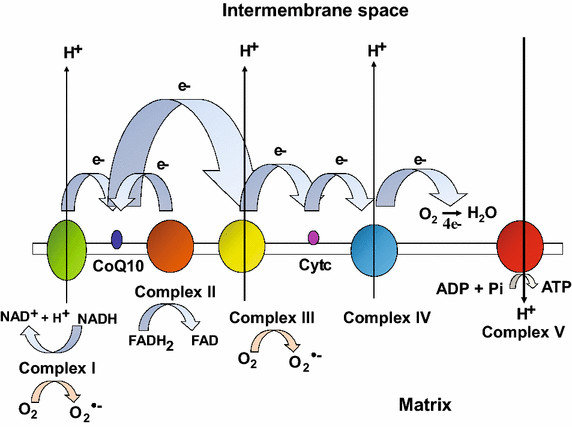
Ilustración esquemática del sistema de fosforilación oxidativa.
Se compone de cinco complejos enzimáticos multiméricos (CI – V).
Complejo I = NADH-ubiquinona óxido-reductasa. también denominado NADH deshidrogenasa
Complejo II = succinato-ubiquinona reductasa
- Único codificado solamente por el ADN nuclear
- Único complejo que NO bombea hidrogeniones (H+)
Complejo III = Ubiquinona-Citocromo C óxido-reductasa
Complejo IV = Citocromo c oxidasa
Complejo V = ATP sintasa
La energía producida hasta ahora en las fases anteriores (glucólisis, ciclo del ácido tricarboxílico (o ciclo de Krebs, electrones ricos en energía) almacenada y transportada por las 10 moléculas NADH y 2 moléculas de FADH2 transfieren esos electrones a estos Complejos multienzimáticos, llamados cadena de transporte de electrones.
- El NADH entra en la cadena de transporte de electrones mitocondrial (ETC) y dona 2 electrones (e-) y un hidrogenión (H+) y se oxida a NAD+ sus e- llegan al Complejo I que pasa por una serie de reacciones redox (reducción y oxidación), creando una bomba de protones.
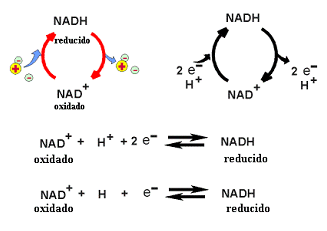
- El FADH2 entra y se oxidad a FAD y sus electrone (e-) e H+ entran en el complejo II
- Un portador de electrones de membrana interna, coenzima Q10 o ubiquinona acepta un electrón del complejo I o del complejo II, respectivamente, y lo dona al complejo III.
- El citocromo c, otro portador de electrones en el espacio intermembrana, llamado así porque es capaz de ceder 2 electrones y de reducir el oxígeno elemental para formar oxígeno iónico, que luego se combina con los hidrogeniones formando agua (H2O).
- Durante el flujo de electrones, los complejos I, III y IV bombean simultáneamente protones desde la matriz hacia el espacio intermembrana generando un gradiente electroquímico o potencial de membrana (Ψm) a través de la membrana mitocondrial interna.
- La energía en este gradiente es aprovechada por el complejo V (ATP sintasa) para generar ATP a partir de ADP y fosfato inorgánico (Pi).
Aproximadamente el 1–2% de electrones se pueden "escapar" (fugas de electrones) de la cadenas de transporte de electrones I y III y combinarse con el oxígeno para formar una forma muy inestable de oxígeno llamada radical superóxido (O 2 • -), lo que produce especies reactivas de oxígeno (ROS). En bajas concentraciones, la producción de superóxido puede estar involucrada en la transducción de señales celulares, pero a altas concentraciones los radicales causan daño oxidativo debido a su alta reactividad hacia otros compuestos celulares.
Por cada molécula de glucosa metabolizada a CO2 y agua se producen 38 ATP que almacenan 456.000 calorías, mientras que se han liberado 686.000 calorías durante la oxidación completa de la glucosa. Esto supone una eficiencia máxima global de transferencia de energía del 66%. El 34% restante se convierte en calor no pudiéndose ser aprovechado por la célula.
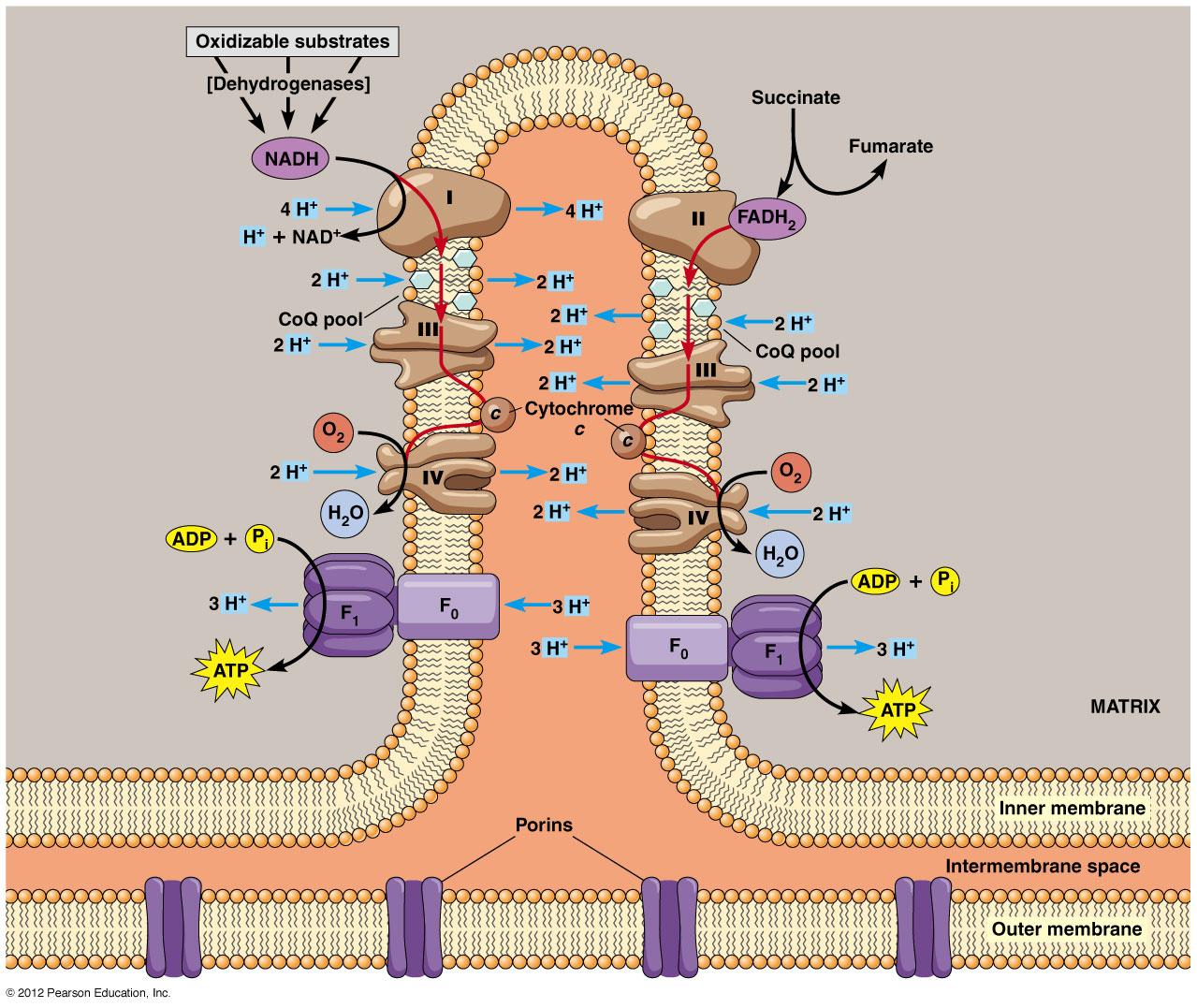
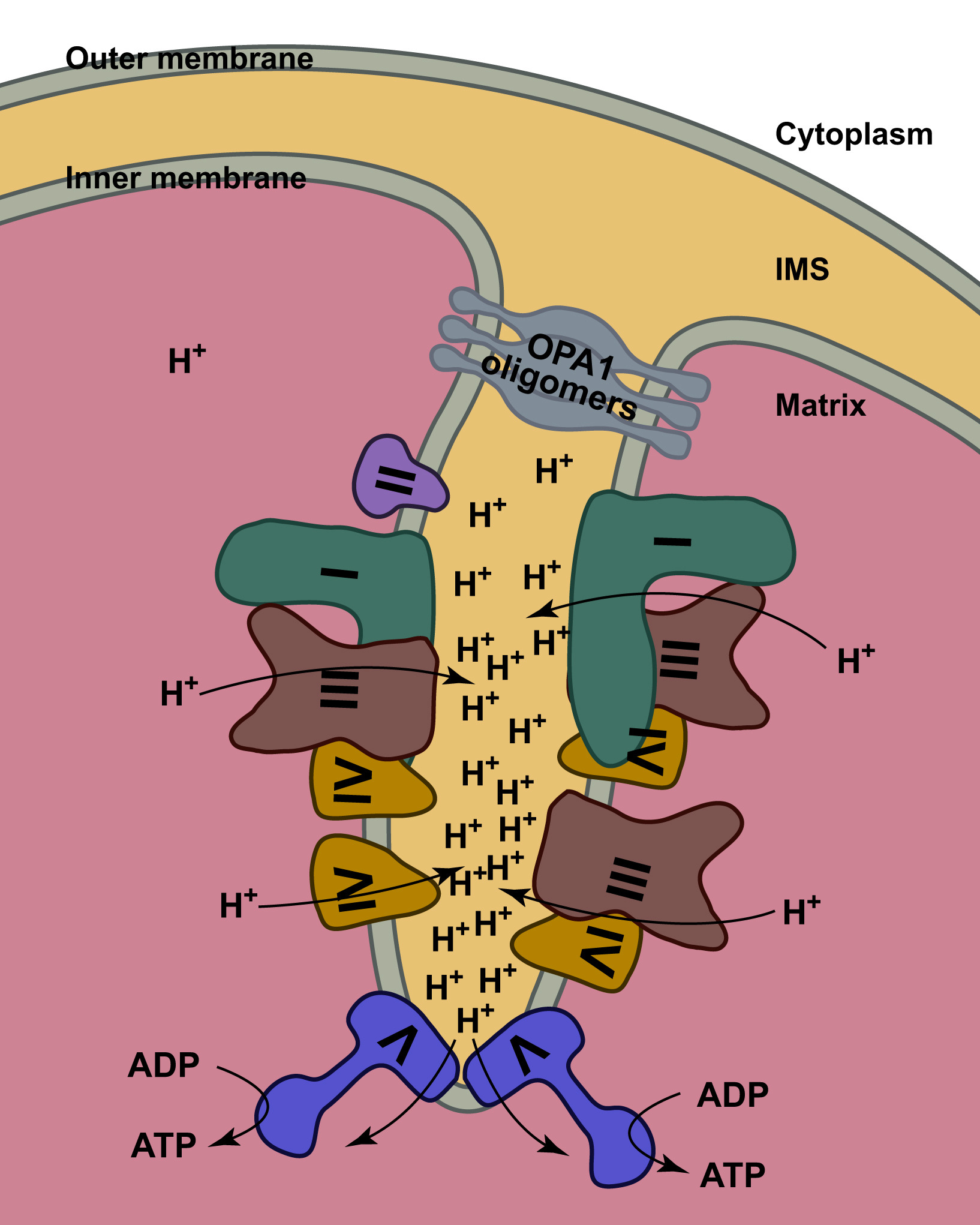
REPRESENTACIÓN ESQUEMÁTICA DE LA LOCALIZACIÓN DE LOS COMPLEJOS RESPIRATORIOS EN LA CRESTA MITOCONDRIAL: SEPARADOS O FORMANDO SUPERCOMPLEJOS I + III + IV y III + IV
PROF.DR. FERNANDO GALAN




